O aparecimento de novas estirpes do vírus PRRS, juntamente com as limitações no uso de antibióticos, está a mudar os paradigmas na produção de suínos. É um facto que, em Espanha, em termos globais, o número de animais perdidos entre as fases de desmame e engorda aumentou 4%, devido a um aumento dos problemas de saúde. Todos os dias conhecemos mais e mais ferramentas para o controlo de muitas das patologias que afectam as explorações, mas temos de adoptar uma abordagem diferente para os problemas habituais e é aqui que reside o trabalho do veterinário de produção: saber como mudar. Para isso, temos de nos apoiar tanto em novas investigações (livros, artigos científicos, etc.) como nos próprios animais.
Actualmente, está bastante documentado que a microbiota intestinal influencia claramente a modulação das respostas inflamatórias e que, portanto, qualquer doença digestiva que leve a alterações na microbiota resulta possivelmente numa redução dos macrófagos alveolares e numa alteração da resposta imunitária Th1 e Th2 (Leucócitos T Helper). Como consequência, pode ocorrer um aumento da resposta inflamatória a nível pulmonar e também um aumento das recidivas e da persistência das doenças pulmonares.

Caso clínico
Trata-se de uma exploração com cerca de 2.000 reprodutoras situada na região de Múrcia. Dado que a exploração ocupa uma superfície de cerca de 100 hectares, as diferentes fases de produção encontram-se distantes umas das outras. Os reprodutores estão num núcleo, os desmames estão situados a 1 km e as engordas estão distribuídos a cerca de 3 km das reprodutoras.
A exploração de reprodutoras é positiva para a PRRS e está actualmente estável. Tem um plano de monitorização mensal com amostragem de línguas de nados-mortos, diferenciando entre leitões de multíparas e primíparas. Esta monitorização consiste na determinação de PCR para PRRS e PCV-2, com o objectivo de controlar ambos os vírus na exploração. Durante este período, as análises das línguas dos nados-mortos foram negativas para PRRS e PCV-2. Quando uma amostra é positiva para o vírus da PRRS, efectuamos a sequenciação por ORF5 para verificar se se trata de uma nova estirpe proveniente de uma entrada lateral do vírus e, portanto, se existem falhas na biossegurança externa.
A exploração é positiva para Brachyspira hyodysenteriae mas, através da utilização de autovacinas, o quadro clínico está controlado e não se observam sintomas nem nas porcas em produção nem nas futuras reprodutoras, que têm a autovacina incluída no seu programa de vacinação. Considera-se que este processo está controlado, embora ocasionalmente apareçam sintomas compatíveis com a disenteria suína nos animais de engorda, quando estes têm aproximadamente 50-80 kg de peso, coincidindo com a perda de imunidade adquirida através das mães.
Na engorda, observa-se um certo grau de mordedura da cauda, o que para nós é um indicador da presença de disenteria, mesmo nos casos em que não observamos um quadro clínico claramente compatível. Se os porcos tiverem uma doença subclínica e, portanto, uma inflamação do cólon, tendem a ser mais nervosos e a abanar a cauda com insistência. Como sabemos, isto é um íman para os companheiros que começam a morder-se uns aos outros. Uma vez estabelecido o comportamento anormal, é difícil de controlar, uma vez que a inflamação crónica induz um comportamento do tipo ansioso.

Início do problema
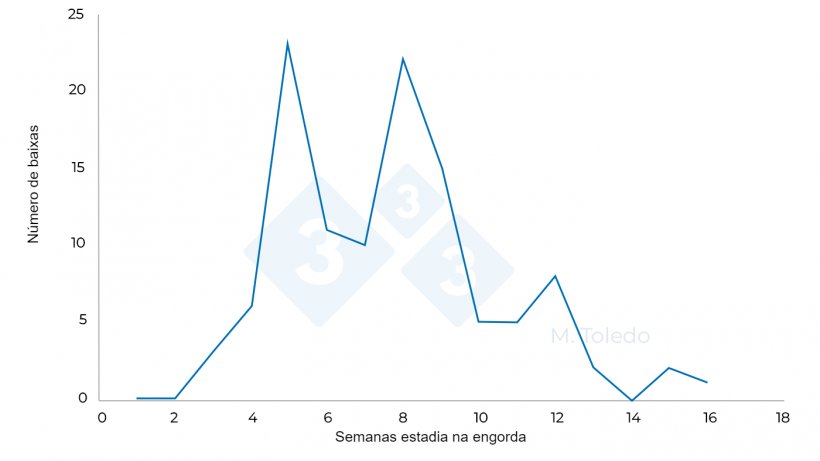
Os animais são transferidos para instalações de engorda de 6000 lugares, que são preenchidas durante 4 semanas consecutivas. Um mês após a entrada dos animais, inicia-se um processo respiratório com dispneia grave e anorexia. Decide-se administrar um tratamento antibiótico com florfenicol solúvel na água de bebida (no primeiro dia associado a um anti-inflamatório para aumentar o consumo de água), mas após o tratamento implementado, as perdas continuam e não se regista qualquer melhoria nos animais. Os pulmões dos animais mortos com grandes áreas de consolidação pulmonar são enviados para o laboratório. Decidiu-se administrar um tratamento antibiótico injectável de Marbofloxacina a todos os porcos (por um lado, para ter a certeza de que cada animal recebia a dose certa e, por outro, para poder chegar ao pulmão com uma concentração eficaz de antibiótico). Apesar de uma melhoria do estado geral dos animais, observa-se uma recaída ao fim de duas semanas e continuamos a não conseguir controlar as perdas que ocorrem. A sintomatologia regressa com a mesma intensidade e continua a gerar um grande número de vítimas (Foto 2 e 3).


Quadro 1. Analíticas de amostras de pulmão e fluidos orais recolhidas na engorda
| Data | Engorda | Amostra | PRRSv | PCV-2 | Gripe tipo A |
|---|---|---|---|---|---|
| Nov-22 | A | Pulmão | PRRSv (Ct 28) | - | - |
| Nov-22 | B | Pulmão | PRSSv (Ct 20) | - | - |
| Nov-22 | C | Fluídos orais | PRRSv (Ct 30) | - | - |
| Nov-22 | D | Fluídos orais | PRRSv (Ct 36) | - | - |
No entanto, tínhamos uma dúvida muito importante: é normal que um agente patogénico recém-introduzido, se tiver uma baixa prevalência, produza doença clínica no final do período de engorda e que, à medida que a sua prevalência aumenta, o faça em animais cada vez mais jovens. No entanto, não foi isso que aconteceu nesta pirâmide, pelo que pensámos que os tratamentos com antibióticos iriam reduzir o impacto da doença, mas não foi isso que aconteceu.
Na altura em que se obteve a sequenciação do vírus da PRRS, verificou-se que se tratava da mesma estirpe, pois havia uma homologia filogenética com a estirpe residente nessa pirâmide. No entanto, na fase de engorda nunca se tinha comportado desta forma. Anteriormente, surgia sintomatologia respiratória, mas era facilmente controlada com tratamento antibiótico (florfenicol).
O que estava a acontecer na linha de engorda para este comportamento anormal?
Neste momento, está a ser considerada uma nova forma de abordar a infecção, uma vez que o Eixo Intestino-Pulmonar está a tornar-se mais conhecido, e sabe-se que o que acontece no intestino afecta a gravidade dos processos respiratórios.
Perguntámo-nos se haveria outra patologia que não fosse pulmonar, mas localizada no intestino, e isolámos Brachyspira hyodesenteriae nas fezes. Este achado não era novo, mas pensámos que estava controlado porque não apresentava os sintomas clássicos da diarreia mucohemorrágica, mas apenas um branqueamento que aparentemente não parecia ter grande significado clínico.
Poderá a presença de Brachyspira hyodesenteriae ser uma das causas da gravidade e persistência dos sintomas clínicos?
HIPÓTESE: "A presença da Brachyspira hyodesenteriae e o seu impacto na microbiota intestinal poderia estar a afectar a modulação das respostas inflamatórias com um aumento da resposta inflamatória a nível pulmonar, e uma redução dos macrófagos alveolares o que estaria a criar um ambiente imunitário em que não seria possível eliminar o vírus da PRRS de forma suficientemente eficaz e favoreceria também um aumento da recorrência e persistência das doenças pulmonares"..
Verificámos que a estirpe isolada de Brachyspira hyodesenteriae continuava a ser a estirpe residente e descobrimos as CMI dos diferentes antibióticos que tínhamos de utilizar para o seu controlo.
Quadro 2. CMI dos diferentes antibióticos para a estirpe de Brachyspira hyodesenteriae isolada.
| CEPA SV22-3448 | |||||
|---|---|---|---|---|---|
| Antibiótico intervalo analisado (μg/ml) |
CMI (μg/ml) |
Interpretação sensibilidade | Intervalo (μg/ml) | ||
| Tiamulina (0,063 - 8) | 0,5 | Intermédia |
≤ 0,25 > 0,25 - ≤ 2 > 2 |
Sensível Intermédia Resistente |
La et al., 2016 |
| Valnemulina (0,031 - 4) | < 0,031 | Sensível |
≤ 0,25 > 0,25 - ≤ 2 > 2 |
Sensível Intermédia Resistente |
La et al., 2016 |
| Tilvalosina (0,25 - 32) | 8 | Intermédia |
≤ 0,25 - < 1,5 > 1,5 - ≤ 36 > 36 |
Sensível Intermédia Resistente |
Pringle et al., 2012 |
| Lincomicina (0,5 - 64) | 32 | Intermédia |
≤ 4 > 4 - ≤ 36 > 36 |
Sensível Intermédia Resistente |
Kirchgässner et al., 2016 |
| Tilosina (2 - 128) | > 128 | Resistente |
≤ 1 > 1 - ≤ 4 > 4 |
Sensível Intermédia Resistente |
La et al., 2016 |
Como se pode ver na tabela 2, a tiamulina parecia ser a melhor opção, mas a nível de campo e com as características físicas da água na Região de Múrcia (má qualidade e alta salinidade), este antibiótico não oferece uma boa eficácia, sendo a lincomicina o ingrediente activo que oferece a melhor cobertura para uma melhor resolução do problema clínico. Procedeu-se ao estabelecimento de um tratamento antibiótico orientado principalmente para o controlo da disenteria suína subclínica.
Conclusão
A abordagem bem sucedida deste caso clínico foi o controlo da disenteria, mesmo que subclínica. Desta forma, o processo respiratório foi gerido de uma forma muito menos agressiva e sem recidivas. O controlo da disenteria levou também a uma redução da ocorrência de novos episódios de mordedura da cauda.
Temos de começar a abordar de forma diferente os processos respiratórios (especialmente o que nos está a causar mais problemas, que é o vírus da PRRS), monitorizando e controlando as condições entéricas que aparecem devido a interacções entre os diferentes agentes patogénicos intestinais que são capazes de produzir disbiose. É importante não considerar estes agentes patogénicos digestivos individualmente, uma vez que existem muitas interacções entre eles (Brachyspira spp, Lawsonia intracellularis, Escherichia coli, etc.). Esta alteração do intestino pode estar a modular a intensidade e a duração dos processos respiratórios e, por conseguinte, a complicar o seu controlo.