Descrição da Exploração
Trata-se de uma Cooperativa que possui 2 unidades produtora de leitões e um Centro de Inseminação Artificial, localizado no Estado do Paraná (Brasil). As UPLs estão localizadas num raio de 60 km uma da outra e da CIA 35 km a UPL 1 e 60km a UPL 2 (Ilustração 1).

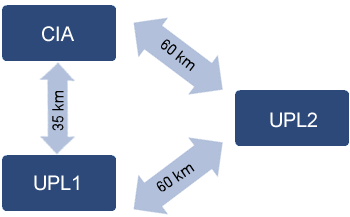
Ilustração 1. Distancia de granjas UPL e CIA.
No mês de março de 2011, ocorreu um relato por parte dos gerentes das Upls, onde o mesmo comunicava o incremento de fêmeas com retorno ao cio (entre os 17 e os 28 dias, cíclico e acíclico, com 22% de retorno de cio) e corrimento vulvovaginal com aspecto mucoso, com coloração de branco a castanho (chocolate) poucas horas após a inseminação artificial. Sendo a maior incidência em nuliparas porém, também acometia as fêmeas com outras ordens de parição. As fêmeas desmamadas são alojadas em jaulas em ambiente climatizado a temperatura de 21 °C e humidade relativa entre 60 -70% seguindo na mesma área no mínimo pelas primeiras sete – oito semanas de gestação.
Este problema aconteceu nas 2 explorações. As visitas de auditoria iniciaram pela CIA, por medidas de biossegurança, e posterior nas UPLs, devido aos protocolos de visitas técnicas que são realizados pela empresa de consultoria. A suspeita clínica foi a presença de micotoxinas, onde a empresa de nutrição se responsabilizou pela recolha de amostras e acompanhamento na quantificação do mesmo, sendo este não detectado nas matérias primas.
Quanto ao estatuto sanitário
Nas UPLs, o efectivo apresenta-se negativo quanto a soroconversão de PRRS e Aujeszky e positivo para Mycoplasma hyopneumoniae. Adoptando nas suas rotinas adequadas medidas de biossegurança lhes permitem um bom controlo sanitário com baixa incidência de sinais clínicos que caracterizem presença de doenças agudas e crónicas.
O programa de reposição das granjas comerciais é realizado através da aquisição de fêmeas F1 desmamadas de origem da exploração própria multiplicadora que tem suas as próprias Bisavós e Avós e a aquisição desse material genético que cumpre as bases de melhoramento ocorre através da aquisição de sémen de avôs e bisavôs através de um programa fechado. O Centro de inseminação da empresa produz 7.500 doses ao mês.
Quanto ao CIA
Trata-se de um CIA moderno semi automatizado que utiliza em seus processos materiais descartáveis. Os varrascos apresentam-se livres de anticorpos de PRRS, Aujesky, Leptospirose, Brucelose. São vacinados a cada 6 meses para Erisipela, Leptospirose e Parvovirose. Estão instalados em baias de 7,5m² em ambiente climatizado a temperatura de 21 °C (com variações entre máxima e mínima de 4 -6°C), humidade relativa de 60 - 70% e luminosidade entre 12 – 14 h.
A sala de recolha apresenta fosso de recolha e as dependências do laboratório estão devidamente separadas as áreas limpa, suja e intermediária. Produz no próprio laboratório água osmoseificada através do osmose reversa na obtenção de purificação da água para produção das doses. Todos os equipamentos são de material de aço inoxidável, e utilizam-se materiais descartáveis para manipulação do sémen. As doses são embaladas automaticamente em embalagens plásticas de tubo.
Visita técnica
Durante a visita ao CIA foram recolhidas amostras de água, sémen puro e diluído, e materiais que fazem parte do processo de manipulação e produção das doses de sémen como abaixo demonstra a tabela 1 com seus respectivos resultados.
Tabela 1. Bacteriologia

| Amostra | UFC / mL – Agente |
| Água recém osmoseificada | Não crescimento de bactérias |
| Água recolhida do homegeneizador com diluente | 36 UFC |
| Laminocultivo Água com diluente | Crescimento e isolamento de Burkholderia cepacia |
| Água com diluente | Crescimento e isolamento de Burkholderia cepacia |
| Homogeneizador Saco/ Hélice | Crescimento e isolamento de Burkholderia cepacia |
| Tubo de recolha – Blister | Não crescimento de bactérias |
| Caneca de repouso para bico doseador | Não crescimento de bactérias |
| Pote do canudo | 10 UFC |
| Bico do dosador | Não crescimento de bactérias |
(UFC) Unidade formadora de colónia
Tabela 2. Bacteriologia sémen diluído
| Amostra | Agente Isolado |
| Sémen diluído – 1 | Burkholderia cepacia |
| Sémen diluído – 2 | Burkholderia cepacia |
| Sémen diluído – 3 | Burkholderia cepacia |
| Sémen diluído – 4 | Burkholderia cepacia |
Resultados
Assim foi verificado que existia uma pré-contaminação bacteriana no tanque do homogeneizador ( na hélice e no próprio saco plástico descartável que reveste o tanque). A contaminação se estabeleceu também nas doses produzidas naquele momento devido a alta concentração bacteriana existente no tanque (saco plástico e na hélice) sendo isolada a mesma cepa da bacteriana encontrada no tanque de diluição.
1ª Conclusão: Não estava sendo descartado o saco plástico do tanque após o uso sendo renovado apenas uma vez por semana. A recomendação consiste em trocar todo material descartável após terminar a produção das doses.
Visita a uma das explorações (UPL 1)
Durante a visita na UPL, foi realizada a recolha da primeira urina nas fêmeas gestantes desprezando os primeiros jactos da urina recolhendo a porção intermediária em frasco estéril mantendo todos os cuidados básicos necessários de higiene durante o procedimento. Em seguida o material foi devidamente condicionado e transportado em refrigeração até o processamento no laboratório.
Na urocultura foi demonstrado que 15% das amostras recolhidas apresentaram crescimento bacteriano identificado pelo crescimento de Burkholderia cepacia. A Burkholderia cepacia é uma bactéria que normalmente é encontrada no solo, água e pode sobreviver por longos períodos em ambientes húmidos. Estudos têm identificado a presença da Burkholderia cepacia em humanos com fibrose cística presente em patologias respiratórias.
Também foi selecionada uma nulipara com presença de secreção vulvovaginal em abundância que na avaliação clinica apresentava todos os parâmetros fisiológicos normais, sem nenhuma indicação de estado febril ou perda de apetite (a temperatura rectal era de 38.7 °C). Sendo a única observação clinica a presença do corrimento mucoso e presença de estrias de muco e hiperemia na mucosa vaginal. A fêmea havia sido recentemente inseminada (recebeu a primeira dose de sêmen no período da manhã e se procedeu à recolha de material no final da tarde).
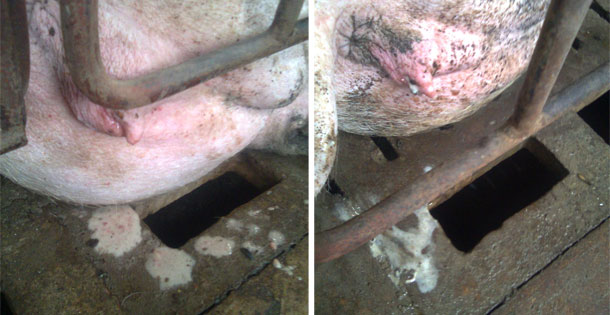
Figura 1. As imagens acima demonstram o corrimento vulvar
Foram recolhidos swabs dessas secreções para tentativa de isolamento bacteriano. Os resultados estão inseridos na tabela abaixo:
Tabela 3. Resultados do isolamento bacteriano
| Amostra | Agente Isolado |
| Mucosa Vaginal | Crescimento e isolamento de Burkholderia cepacia |
| Mucosa da Cervix | Crescimento e isolamento de Burkholderia cepacia |
| Mucosa do Útero | Crescimento e isolamento de Burkholderia cepacia |
| Mucosa da Bexiga | Ausência de crescimento de bactérias |
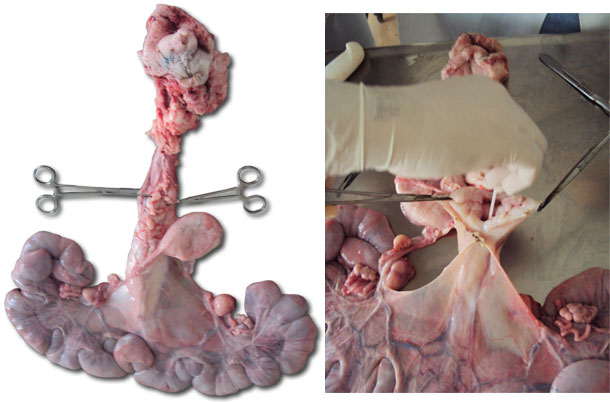
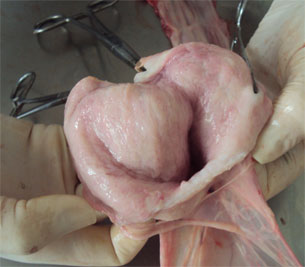
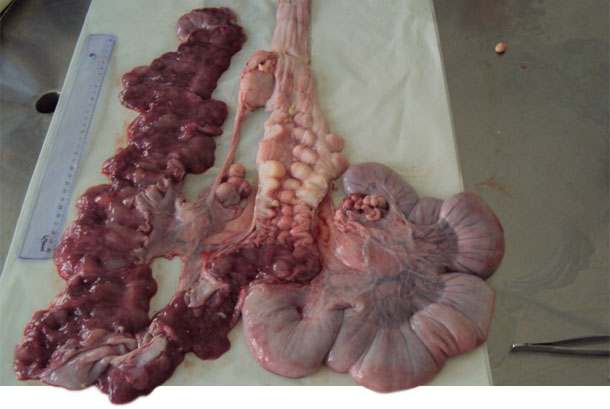
| Figura 2. Aparelho reprodutivo da nulipara | Figura 3. Abertura da cervix para coleta da secreção com swab |
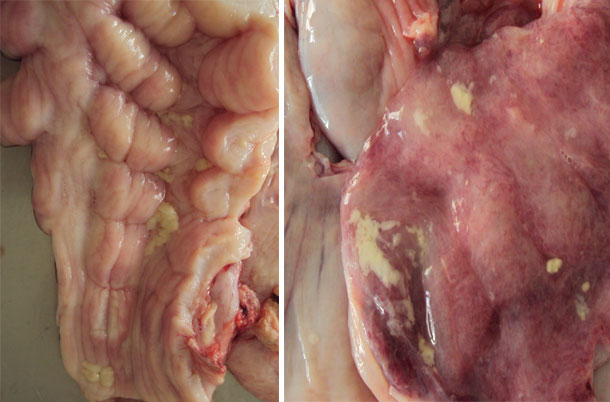
Figura 3. Presença de muco na mucosa da cervix e na mucosa uterina
|
|
Outras fêmeas recém inseminadas que apresentavam os mesmos sinais clínicos foram seleccionadas para recolha de secreções vulvovaginais através de swabs profundos utilizando espéculos descartáveis para melhor abertura da mucosa vaginal e introdução do swab. Na mesma seqüência durante a analise clinica se destacava com os mesmos sinais clínicos uma fêmea nulipara com histórico de completa inseminação a qual foi seleccionada para sacrifício e necropsia. Sendo recolhido todo aparelho urogenital que quando aberto se procedeu a coleta das estrias do muco purulento da cervix, vagina e cornos uterinos para cultivo e isolamento bacteriano.
Conclusão: Em todo material recolhido para isolamento bacteriano ocorreu crescimento da mesma bactéria Burkholderia cepacia.
Estratégias de maneio que foram adoptadas:
- Recorrer a medicação injectável com ceftiofur nas fêmeas com problemas;
- Refugo das fêmeas que retornaram cio com presença de corrimento;
- Adoptou o processo de autoclavar todo material do laboratório que apresentou contaminação;
- Utilizar no tanque de diluição uma bolsa descartável por dia;
- Aumentou os cuidados básicos de higiene com o pessoal de recolha e laboratório. Passando a utilizar máscaras descartáveis nas vias respiratórias dos funcionários durante as actividades de preparação das doses de sémen;
- Visitas ao Centro e às explorações a cada 15 dias com recolha de material de todas as fases do processo de produção de sémen até que as condições voltassem à normalidade;
- Imediatamente evitou-se armazenar as doses de sémen por mais de 72 horas;
- O problema no laboratório foi solucionado em três semanas, mas as perdas de resultados tiveram duração de 10 semanas.
No diluente utilizado tinha presente antibióticos, no qual o mesmo apresentou resistência frente a bactéria no antibiograma. Conforme pode ser visualizado abaixo. E foi solicitado a adição de moléculas antimicrobianas sensíveis a B. cepacia nos diluentes.
Tabela 4. Antibiograma-RG 131
| Antibióticos |
Burkholderia cepacia (água com diluente) |
Burkholderia cepacia (sémen 88645 diluído) |
||
| Halo de inibição | Sensibilidade | Halo de inibição | Sensibilidade | |
| Amoxicilina 10 mcg | 6 mm | R | 6 mm | R |
| Ampicilina 10 mcg | 6 mm | R | 6 mm | R |
| Apramicina 15 mcg | 16 mm | S | 16 mm | S |
| Ceftiofour 30 mcg | 26 mm | S | 26 mm | S |
| Colistina 10 mcg | 6 mm | R | 6 mm | R |
| Enrofloxacina 5 mcg | 26 mm | S | 26 mm | S |
| Espectinomicina+Lincomicina 100+9 mcg | 14 mm | R | 14 mm | R |
| Florfenicol 30 mcg | 16 mm | I | 16 mm | I |
| Gentamicina 10 mcg | 6 mm | R | 6 mm | R |
| Neomicina 30 mcg | 6 mm | R | 6 mm | R |
| Norfloxacina 10 mcg | >30 mm | S | >30 mm | S |
| Penicilina G 10 um | 6 mm | R | 6 mm | R |
| Sulfazotrim 25 mcg (Sulfametazina+Trimetropim) | 6 mm | R | 6 mm | R |
LEGENDA: S = Sensível R = Resistente I = Intermediário
Método: Difusão em ágar
Referência: CLSI (Clinical And Laboratory Standards Institute)