Existem cinco tipos principais de hepatite vírica em seres humanos designadas como hepatitis A, B, C, D e E. A hepatite E é causada pelo vírus da hepatite E (nome taxonómico HEV, Orthohepevirus A), um vírus ARN não envolvido, pertencente à família dos hepeviridae. Segundo as estimativas da OMS, há aproximadamente 20 milhões de infecções por HEV por ano em pessoas de todo o mundo. A transmissão deste vírus ocorre com frequência através de via oro-fecal, com frequência associada a más condições de higiene e água potável contaminada. Nos seres humanos, o HEV tende a estar associado a uma infecção sub-clínica leve a curto prazo. Os sinais da hepatite E aguda podem incluir icterícia, fadiga e náuseas e costuma manifestar-se como uma doença com hepatite que regride espontaneamente. A progressão para uma insuficiência hepática severa fulminante pode ocorrer em certos grupos de alto risco. Além dos seres humanos, o HEV também foi identificado numa ampla gama de animais domésticos e selvagens. No entanto, a informação sobre a importância clínica do HEV nas diferentes espécies animais continua a ser muito limitada. As estirpes de HEV podem ser divididas em oito genótipos diferentes (tabela 1). Os genótipos 1 e 2 estão limitados aos seres humanos e associados com epidemias. Todos os outros genótipos nesta espécie foram identificados numa gama crescente de mamíferos. Do ponto de vista da saúde pública, sabe-se que os genótipos 3, 4 e 7 podem cruzar barreiras entre espécies e, portanto, são os que têm maior potencial zoonótico. Os casos esporádicos e agrupados de hepatite E em seres humanos foram relacionados com o consumo de carne contaminada seja crua ou insuficientemente cozinhada de porco, javali ou veado e, mais recentemente, leite de camelo.
Tabela 1: Classificação genotípica do vírus da hepatite E (HEV) ou Orthohepevirus A, incluíndo o intervalo hospedeiro, a distribuição geográfica e o potencial zoonótico.

| Genótipo | Intervalo de hospeiros | Distribuição geográfica | Potencial zoonótico |
| 1 | Humanos | Ásia | |
| 2 | Humanos | México, África | |
| 3 | Humanos Porcos, javali Coelhos Veado Mangustos Alce Cabras Vacas |
Global | Sim |
| 4 | Humanos Porcos, javali Veado Cabra Vaca |
Ásia, Europa | Sim |
| 5 | Javali | Japão | Provável |
| 6 | Javali | Japão | Provável |
| 7 | Camelo, Humanos | Médio Oriente | Sim |
| 8 | Camelo Bactriano | Médio Oriente | Não |
| Não clasificado até à data | Alce | Suécia | Não |
| Garça | Hungria | Não | |
| Peneireiro | Hungria | Não |
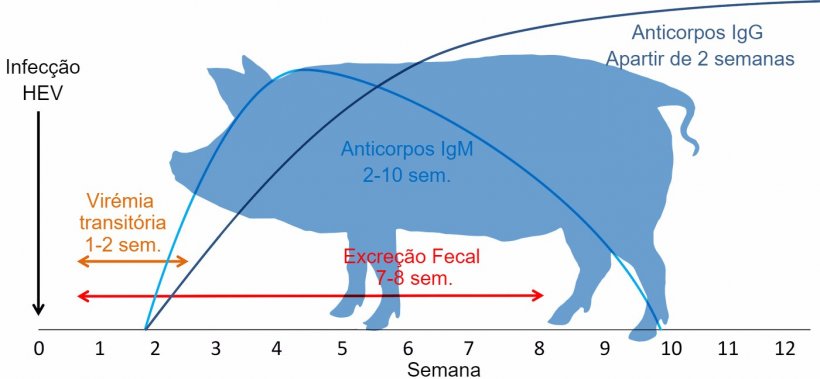
O HEV foi identificado pela primeira vez em porcos em 1997 e, até à data, é aceite que os genótipos 3 (com mais frequência), 4, 5 e 6 circulam em porcos e javalis (tabela 1). A infecção por HEV em porcos parece ser ubíqua. A maioria das explorações de suíno nas principais zonas produtoras de porcos do mundo são seropositivas com anticorpos anti-HEV. Normalmente, os porcos apresentam uma infecção sub-clínica e não têm lesões macroscópicas no fígado, mas podem ter leves lesões microscópicas de hepatite multifocal linfoplasmocítica. Os porcos são infectados por contacto directo com fezes de porcos infectados ou por exposição a água e/ou ração contaminados com HEV. Os porcos infectados geralmente têm uma virémia curta de 1-2 semanas de duração (fig. 1). O tempo que passa desde a infecção com o vírus até à excreção através das fezes pode variar de 1 a 4 semanas. A resposta através de anticorpos anti-IgM pode ser detectada pela primeira vez 1-3 semanas depois da infecção e pode durar até 10 semanas depois da infecção. A resposta anti-IgG tende a ser detectável às 1-3 semanas depois da infecção e pode persistir durante muitos meses, inclusive anos (fig. 1). A maioria dos leitões recém-nascidos têm anticorpos adquiridos de forma passiva que duram até aos 2-3 meses de idade e considera-se que conferem protecção. Uma vez que estes anticorpos diminuem, a maioria dos porcos infectam-se com HEV e desenvolvem uma resposta imunitária eficaz.
Os porcos e os javalis são considerados reservatórios importantes para as infecções nos humanos. A transmissão aos seres humanos ocorre via contacto directo, consumo de carne de porco crua ou insuficientemente cozinhada ou de produtos do javali, como as salsichas. Diferentes investigações de campo descobriram que cerca de entre 2% e 11% dos fígados de porco comercializados nos supermercados do Japão, Europa e Estados Unidos eram positivos ao ARN do VHE e foi confirmada a infectividade do VHE em modelos animais. Também é possível a transmissão indirecta por contacto produzida através da exposição a chorumes de porco infectado com HEV. Foi identificado HEV em morangos cultivados no Canadá, em framboesas congeladas e vegetais produzidos para saladas na Europa, provavelmente devido a contaminação pela água de rega. Além disso, os genótipos 3 e 4 do HEV também podem ser identificados com frequência em mariscos, incluíndo ostras, ostras planas, mexilhões e ameijoas. Suspeita-se que esta contaminação é produzida pela bioacumulação a partir da água e a concentração do vírus nos seus tecidos digestivos.
Nos últimos anos na China foi comercializada uma vacina para a população humana contra a HEV e parece ser eficaz. Ainda que tenha sido desenvolvida e testada uma vacina para HEV nos porcos, este produto não está disponível comercialmente já que o interesse da indústria suína nesta vacina é limitado ao presente. Os seres humanos têm mais probabilidades de estar expostos a HEV agora que a carne de porco crua ou pouco feita e os produtos de javali são cada vez mais populares em certos grupos demográficos, os órgãos de porco são considerados com frequência para uso em transplantes humanos e os produtos farmacêuticos derivados do porco são cada vez mais utilizados em medicina humana. Dado que o risco de exposição ao vírus da Hepatite E parece aumentar na população humana, está a surgir uma oportunidade para a produção e certificação de produtos cárneos livres do vírus da hepatites E, especialmente a carne de porco.



