Descrição da exploração
Trata-se de uma exploração de multiplicação de 250 porcas na região polaca da Grande Polónia, em que todas as porcas que servirão para a reposição mantêm-se na exploração até que atinjam os 100 kg. Os machos e as marrãs não seleccionadas vendem-se para um engordador após o desmame. Utiliza-se inseminação artificial. Trabalha-se com grupos tecnológicos de 10 porcas gestantes e os leitões desmamam-se aos 28 dias, mantendo o sistema "tudo dentro-tudo fora". Aproximadamente são desmamados 6200 leitões anualmente.

No momento do aparecimento do caso as condições ambientais da exploração eram boas e o estado sanitário considerava-se como muito alto: era negativa a Brachyspira hyodysenteriae, Salmonella spp. e Pasteurella multocida toxigénica, PRRSV, Actinobacillus pleuropneumoniae, Mycoplasma hyopneumoniae, Leptospira spp. e só positiva a Bordetella bronchiseptica e Lawsonia intracellularis. Tampouco se tinham descrito casos de PMWS. A rotina profiláctica nas reprodutoras incluía vacinação contra a colibacilose (em nulíparas às 8 e 3 semanas antes do parto e em porcas às 3 semanas) e contra erisipelas e parvovirose (nulíparas aos 5,5 e 6,5 meses de idade e nas porcas às 3 semanas antes do parto). Não se tinha vacinado contra a PCV2.
Aparecimento do caso
Durante a primeira visita observou-se morte súbita de animais, também se observaram animais com um profuso edema facial nas orelhas e região peitoral (fig. 1), bem como um aumento da temperatura corporal até aos 41,5 ºC. Nalguns animais também se apreciaram sintomas neurológicos (opistótono, posição lateral, movimentos de pedalar com as patas). Inicialmente os sintomas observaram-se num grupo de nulíparas de 70-100 kg de peso. A morbilidade aumentou até mais de 15 % e a mortalidade ascendeu a mais de 6 %. Durante o mês seguinte observaram-se sintomas similares, mas com uma intensidade ligeiramente menor, e que afectaram animais mais jovens – transição e nulíparas até 70 kg. Nas semanas seguintes observaram-se sintomas parecidos (excepto os neurológicos) em porcas desmamadas e na maternidade e lactação.
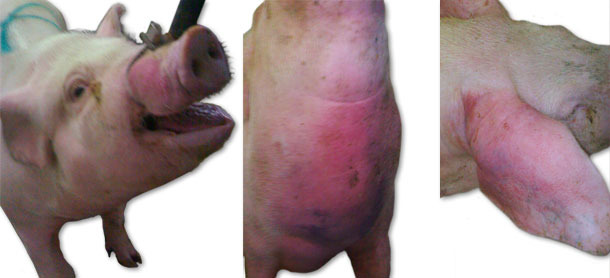
Fig. 1. Sintomas de edema.
Necropsia e testes laboratoriais
Enviaram-se quatro animais doentas para o laboratório. Apresentavam sintomas clínicos como sejam um grande edema com fóvea nas partes mais baixas, acumulação subcutânea de fluido na área do esterno em dois leitões desmamados (fig. 3) e temperatura de 41,0 a 41,3 ºC. A necropsia mostrou uma infiltração subcutânea gelatinosa, especialmente nas zonas mais baixas (fig. 2, 3), pericardite serofibrinosa (fig. 4) e pleurite.
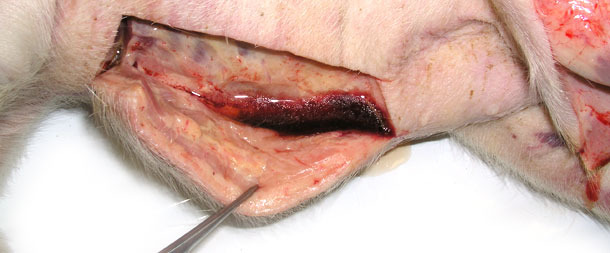
Fig. 2. Inchaço do tecido subcutâneo, emerge uma grande quantidade de fluido após incisão da pele na zona baixa do corpo.
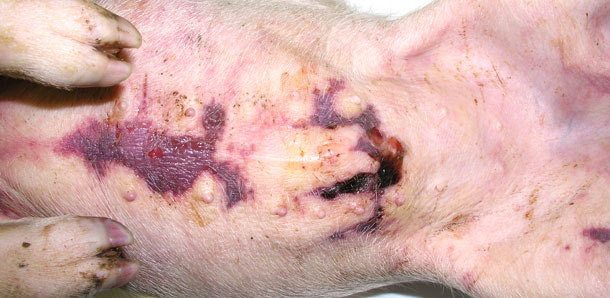
Fig. 3. Acumulação de fluido sob a pele na área esternal.
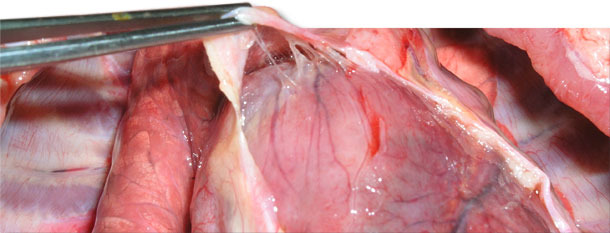

Fig. 4. Fibrina delicada e frágil entre o epicárdio e o saco pericárdico.
Após a avaliação patológica, realizou-se o exame bacteriológico. Devido a não haver coxeiras nem sintomas nervosos nos animais examinados, não se recolheram amostras das articulações nem de fluido cerebroespinal. O material analisado foi recolhido asépticamente e as amostras com zaragatoa foram recolhidas pouco tempo depois de se abrirem as cavidades corporais.
As amostras foram semeadas em agar de sangue de cavalo com Staphylococcus epidermidis e em agar McConkey. A identificação realizou-se com testes bioquímicos (Vitec) ou mediante PCR.
Resultados laboratoriais
Os estudos bacteriológicos só mostraram crescimento de Haemophilus parasuis (H. parasuis). As colónias eram muito pequenas (como picadas de alfinete), não hemolíticas, com satelitismo (aumento das colónias) cerca da estria de Staphylococcus epidermidis (fonte de NAD).
As zaragatoas recolhidas das alterações patológicas (leitões desmamados) analizaram-se mediante PCR. Os resultados apresentam-se na tabela 1.
Tabela I. Diagnóstico laboratorial de Haemophilus parasuis a partir de superfícies serosas e soro.
| tecido | leitão 1 | leitão 2 | leitão 3 | leitão 4 |
| Isolado + PCR / PCR tecido | ||||
| pleura | +/+ | +/+ | +/+ | +/+ |
| pericárdio | +/+ | +/+ | +/+ | +/+ |
| peritoneu | -/- | +/+ | -/- | -/- |
| soro | +/+ | -/- | -/- | -/+ |
Confirmou-se a presença de H. parasuis nas lesões típicas de Glässer. Também se identificou a bactéria, o seu ADN (PCR), no soro, o que demostrou que dois dos quatro leitões analisados apresentavam bacteriémia.
Após a detecção de H. parasuis nos quatro leitões necropsiados recolheram-se 20 zaragatoas nasais de desmamados, nulíparas e porcas para comparar as estirpes dos animais doentes com a dos sãos (portadores). Realizou-se um isolado e identificação dos microorganismos das zaragatoas (identificação bioquímica e confirmação final da estirpe mediante PCR).
Analisaram-se dez isolados de H. parasuis – quatro dos animais necropsiados e seis dos sãos – mediante caracterização molecular por ERIC PCR (fig. 5). Todos os isolados que se obtiveram dos animais doentes tinham o mesmo perfil ERIC PCR. Curiosamente, encontraram-se estirpes idênticas nas amostras nasais de dois dos seis animais sãos. Os quatro restantes tinham distintas estirpes de H. parasuis na cavidade nasal, caracterizados por distintos perfis ERIC PCR.

Fig. 5. Dendrograma que compara as estirpes isoladas de H. parasuis mediante ERIC PCR.
Tratamento
O tratamento consistiu em amoxicilina + ácido clavulânico i.m. nos animais com sintomas clínicos e na implementação de um tratamento metafiláctico com amoxicilina na água de bebida (14 dias, 20 mg/kg pv) no resto dos animais. Este tratamento teve um resultado terapêutico permanente.
Conclusões
Nas explorações com elevado estado sanitário, a infecção por H. parasuis apresenta-se frequentemente de forma aguda, afectando animais de qualquer grupo etário. Os sintomas como febre, apatia, problemas respiratórios, dor ao pressionar os músculos abdominais (defesa muscular), inflamação das articulações e coxeiras são característicos desta forma de Glässer. Também podem observar-se sintomas nervosos e edema subcutâneo, como sucedeu neste caso.
As alterações patológicas descritas neste caso são característicos de uma inflamação aguda serofibrinosa. Estas alterações não são patognomônicas, pelo que o diagnóstico deve basear-se na análise laboratorial.
A específica localização do edema nas partes baixas do corpo, assim como o seu carácter de depressão (fóvea) faz pensar numa falha cardíaca (edema cardíaco), concretamente numa falha cardíaca congestiva com o consecuente paragem do sangue na circulação sistémica. Sem embargo, esta conclussão não é concordante com a presença confirmada de H. parasuis no tecido subcutâneo neste caso concreto. Isto poderia sugerir inchaço inflamatório causado directamente pelo agente bacteriano. Isto pode ser explicado pela bacteriémia: detectou-se presença da bactéria no tecido subcutâneo, procedente de vasos sanguíneos danificados.
A possibilidade de diferenciar entre estirpes de H. parasuis circulantes na exploração pode ser importante já que a epidemiologia do H. parasuis é complexa e a infecção que causa é um processo dinâmico. Por isso, utilizam-se com frequência várias técnicas de tipagem, o que permite identificar entre distintas espécies (ERIC PCR). Em explorações com um bom estado sanitário predominam certas estirpes que podem causar a doença. No caso descrito demonstrou-se que seis isolados tinham o mesmo perfil ERIC PCR e pertenciam a uma mesma estirpe patogénica de H. parasuis. A sua presença também se confirmou em animais clinicamente sãos. Este facto e o efeito terapêutico permanente do antibiótico (sem vacinação), poderia indicar uma imunidade crescente na exploração contra novos casos clínicos pela mesma estirpe patogénica.