É bem sabido que há uma complexa rede de sinais que têm implicações no sistema imunitário e no neuroendócrino, que tem um papel crítico na modulação da resposta inflamatória e imunológica ante perigos ambientais (p.ex. agentes patogénicos, factores nutricionais e/ou ambientais) que implicam uma resposta sistémica.
O objectivo é a manutenção da homeostase, o equilíbrio dinâmico no qual as alterações contínuas estabelecem as condições óptimas para a sobrevivência. A comunicação dos múltiplos sectores garante a manutenção da homeostase e, portanto, da saúde.

O sistema imunitário, endócrino e o sistema nervoso central comunicam entre si através de vias anatómicas e hormono-neuropéptidas.
Os nervos eferentes do sistema nervoso simpático inervam os órgãos linfóides primários e secundários; foi demonstrado que a adrenalina e a noradrenalina activa o eixo hipotálamo-hipófise-suprarrenal (HPA - hypothalamus-pituitary-adrenal) e actuam nos receptores β2 adrenérgicos leucocíticos.
As células imunitárias expressm receptores para muitas hormonas (por exemplo, hormona adrenocorticotrópica, prolactina, hormona do crescimento (Growth Hormone GH), leptina, glucocorticóides, estrogénios e testosterona, neurotransmissores e neuropéptidos como o VIP, substância P, norepinefrina, somatostatina e neuropéptido Y). Do mesmo modo, os tecidos endócrinos e nervosos apresentam receptores específicos para as citoquinas derivadas do sistema imunitário.
Dentro deste âmbito, também está claro que as funções das células imunitário podem ser alteradas pelas hormonas neuroendócrinas e que as células imunitários têm a capacidade de produzir hormonas com uma resposta neuroendócrina funcional.
As hormonas e as citoquinas, em particular as citoquinas pro-inflamatórias e reguladoras, são os principais actores desta conversa coordenada. A sua acção traduz-se numa melhoria da imunidade inata, um controlo da inflamação com um aumento na eficácia da resposta imunitária. Com efeito, também se inicia em resposta a um desafio patogénico para restabelecer a homeostase. Pelo contrário, uma desregulação desta resposta neuroimune pode afectar negativamente a resposta imunitária contra os agentes patogénicos e a eficiência metabólica.
Neste sistema de "verificação e equilíbrio", a evidência emergente aponta para um papel fundamental da microbiota intestinal. A microbiota intestinal interage estreitamente com o principal sistema neuroendócrino do corpo que controla vários processos corporais em resposta ao stress, o eixo hipotalâmico-pituitário-adrenal (HPA). Esta interacção é de fundamental importância já que vários transtornos do eixo microbiota-intestino-cérebro podem-se associar à desregulação do eixo HPA e do sistema imunitário intercorrelacionado.
A activação do eixo HPA e a secreção de glucocorticóides é uma das principais vias neuroendócrinas para controlar a inflamação local e sistémica.
Contudo, a prolactina e a GH também estão envolvidas no desenvolvimento e na eficácia da resposta imunitária. São sinais que facilitam a proliferação, diferenciação e função das células imunocompetentes para estímulos antigénicos específicos mediante uma acção endócrina e paracrina. Com efeito, ambas as hormonas, que são idênticas às hormonas das glândulas endócrinas, são sintetizadas, armazenadas e secretadas por células imunitárias.
O tecido Adiposo Branco desempenha um papel fundamental na rede de neuroimunidade que vincula o estado nutricional, o metabolismo e o equilíbrio energético para manter a homeostase corporal. Os produtos que se sintetizam principalmente no tecido adiposo conhecem-se como adipocinas e incluem factores anti-inflamatórios e pró-inflamatórios, como as citoquinas clássicas, mas também hormonas específicas. As principais hormonas, a leptina e a adiponectina, também foram identificadas como actores importantes na intercomunicação entre o sistema endócrino e o sistema imunitário.
A leptina não só regula a ingestão de alimentos e o metabolismo, como também estimula a proliferação e a sobrevivência de precursores linfóides e o desenvolvimento de células T no timo. Também pode melhorar a resposta Th1 aumentando a produção de IL-2 e IFN-by pelas células T e pelos macrófagos.
A adiponectina inclui múltiplas isoformas e é a adipocina mais expressada. A adiponectina, de elevado peso molecular, actua principalmente como um regulador anti-inflamatório mediante a supressão da diferenciação e da activação clássica dos macrófagos M1 mediante regulação negativa das citocinas pró-inflamatórias, ou seja, TNF-α e IL-6, actuando nos receptores 1 de adiponectina. As isoformas de menor peso molecular parecem ter um papel pró-inflamatório ao aumentar a actividade das moléculas pró-inflamatórias. (Tong et al., 2011; Gomez et al., 2011) (figura 1)
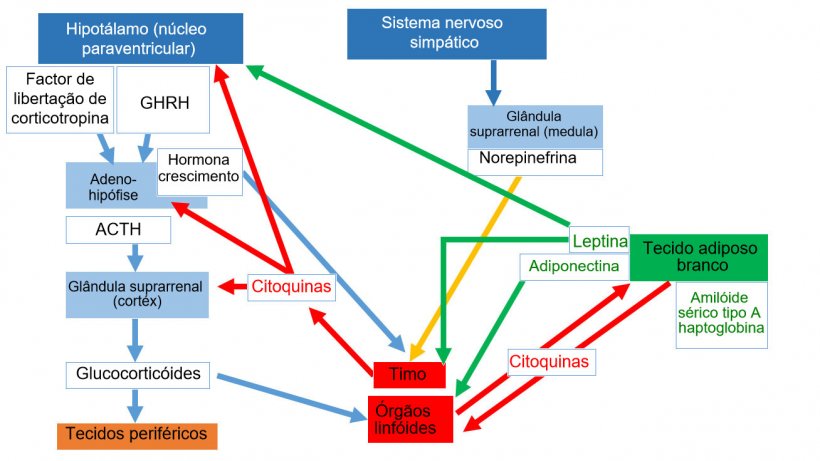
Vários factores stressantes da produção intensiva de suínos, como as práticas de maneio, factores de stress ambiental, factores nutricionais, o desmame, as misturas de animais, as lutas e o transporte podem influir negativamente na resposta imune em termos de eficiência funcional.

É evidente que as primeiras semanas de vida constituem o período mais crítico para os leitões porque o desenvolvimento do sistema imunitário e a sua eficiência aumentam progressivamente. Com efeito, durante o período neonatal, os leitões podem estar expostos a factores stressantes físicos e psicológicos e a infecções que podem influir directamente na eficácia da resposta imunitária.
O desmame é um dos eventos mais stressantes que pode predispor a disfunções do sistema imunitário e intestinal, comprometendo seriamente a saúde, o crescimento e o consumo de alimento, particularmente durante a primeira semana após o desmame.
Do mesmo modo, as infecções são os principais factores que contribuem para a redução do rendimento nos animais de produção durante o crescimento. As infecções persistentes/subclínicas também podem afectar negativamente o rendimento do crescimento influindo no eixo hormonal, no metabolismo tissular e na eficiência nutricional.
Durante a infecção, a activação do eixo HPA e a secreção de glucocorticóides podem influenciar tanto na gravidade como no impacto metabólico da infecção.
Com efeito, uma inflamação descontrolada, com dano tissular potencial, depende de uma interacção complexa entre os níveis de glucocorticóides, a sua actividade periférica e, principalmente, os níveis e a persistência de citoquinas pró-inflamatórias (TNF-a, IL-1β, IL-6, IL -15).
O eixo HPA, a activação/desregulação do eixo do factor de crescimento insulínico tipo 1 (IGF1) e os níveis alterados de citoquinas sistémicas podem induzir alterações metabólicas. No início da infecção/inflamação, várias alterações metabólicas (aumento da GH) podem favorecer uma resposta imune inata eficiente (energia desviada para a activação do sistema imunitário). De seguida, produz-se um desacoplamento entre os níveis de GH e IGF-1 com supressão do eixo GH, resistência hepática e esquelética à GH e inibição da actividade de IGF-1 nos tecidos periféricos (Soendergaard et al., 2017). Além disso, os níveis elevados de glucocorticóides e citoquinas pró-inflamatórias (ou seja, IL-1, TNF-α e IL-6) induzem uma redução da ingesta de alimento, um balanço energético negativo com catabolismo tissular, degradação de proteínas e aminoácidos e uma redução da bio-disponibilidade e secreção de oligoelementos (p. ex., Zn e Cu).
Tabela 1. Sinal principal da comunicação imune-neuroendócrina
| Hormonas | Glucocorticóides |
|
| Hormona do Crescimento (GH) |
|
|
| Leptina |
|
|
| Adiponectina |
|
|
| Citoquinas | IL-1, TNFa, IL-6 |
|






















